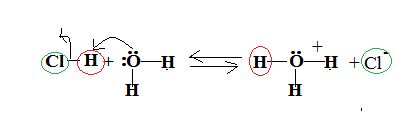La teoria di Lewis permette un ampliamento delle classi degli acidi e delle basi. Tali teoria afferma che gli acidi sono le specie che possono accettare una coppia di elettroni; si dicono basi le specie che possono mettere a disposizione una coppia di elettroni libera da legami.
Le specie acide e basiche possono essere sia molecole neutre sia ioni. Lo ione , per esempio è un acido secondo Lewis perchè può accettare un doppietto elettronico da un donatore, come l’acqua o l’ammoniaca: nel primo caso si forma lo ione idronio, mentre nel secondo lo ione ammonio.
Un esempio è il seguente:
Molti cationi metallici di transizione si comportano da acidi di Lewis accettando i doppietti elettronici delle molecole di acqua e trasformandosi in ioni complessi che possono a loro volta reagire con l’acqua.
Vedi programma di chimica